研究の概要
研究内容: 生理活性タンパク質の構造と機能の解明ならびに組換えDNA技術を用いた高機能人工タンパク質の開発
生理活性タンパク質の構造と機能の解明ならびに組換えDNA技術を用いた高機能人工タンパク質の開発
人間の細胞にはおよそ2.3個の遺伝子が存在していますが,それらの大部分はタンパク質の設計図であることがわかっています。タンパク質は20種類のアミノ酸が数百個以上つながった鎖からできており,酵素,ホルモン,筋肉,皮膚など体の中のさまざまな物質を作り出す大事な役割を果たしています。私たちの研究室では,このように多才な生体物質であるタンパク質の構造と機能をいろいろな測定機器を用いて調べるとともに,大腸菌などの微生物を用いて,遺伝子組み換えタンパク質を合成することによって,有用な機能をもつ新しい人工タンパク質を開発する研究を行っています。
1.糖結合タンパク質(レクチン)の構造・機能解析
細胞表面には,様々な大きさや構造をもつ糖鎖が存在しており,細胞間の相互作用や免疫などの生体防御機構において重要な働きをしています。このような複雑な構造をもつ糖鎖は,特異的な糖結合タンパク質であるレクチン(lectin)によって認識されることによってその役割を果たすことができます。本研究室では,このように生体内で重要な働きをしているレクチンを様々な生物から単離するとともに,その構造と機能を生化学的手法やX線結晶構造解析を用いて明らかにするとともに,それら遺伝子工学的に微生物で発現することにより,これまでにない新規な活性や特性をもつ人工レクチンの研究を行っています。
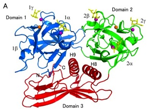
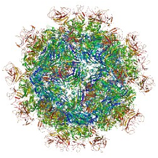
一例として,海産無脊椎動物グミ(Cucumaria echinata)が持っているカルシウムイオン依存性(Ca2+を用いて糖を認識する)レクチンの一つであるCEL-IIIの立体構造を下に示します。グミ(Cucumaria echinata)は九州北部の海底に大量発生している棘皮動物(ナマコの一種)で,その体液中には強い溶血活性を示すカルシウム依存性レクチンCEL-IIIが含まれています。これまでの研究から,CEL-IIIは赤血球膜表面の糖脂質と結合した後に立体構造を変化させ,膜の中で会合することにより溶血を引き起こすことが明らかになっています。このような作用は細菌が持つタンパク質性毒素などとも共通する作用であり,現在どのような立体構造変化が細胞膜との相互作用に関係しているのかをX線結晶構造解析などの手法をもとに研究しています。

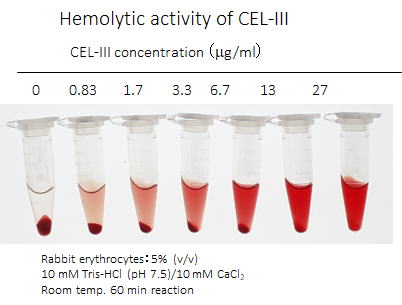
グミの体液中には強い溶血活性を示すCEL-IIIというレクチンが存在しており,グミが魚などから身を守るための毒素として作用しています。このCEL-IIIを精製してその構造や活性を調べた結果,下の図のようには赤血球表面のガラクトースという糖に特異的に結合した後,CEL-IIIの立体構造(コンフォメーション)が大きく変化し,細胞膜表面で七量体から成る膜貫通ポア(小孔)を形成することによって細胞を破壊していることが明らかになりました。
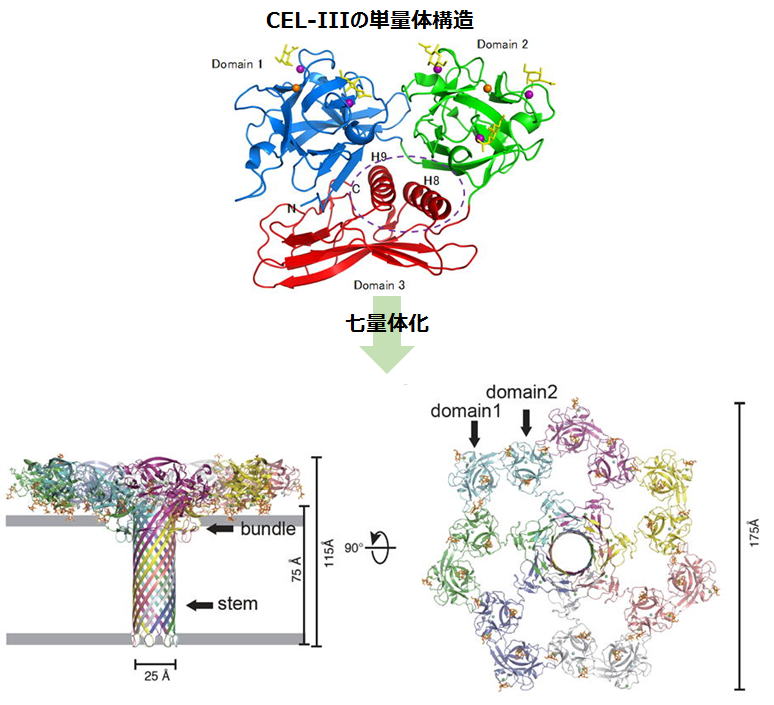
CEL-IIIは通常,分子量64,500の単量体として存在していますが,細胞表面のガラクトース含有糖鎖と結合することにより,大きく立体構造を変化させ,上の図のような細胞膜貫通ポアを形成します。このポアの中心を通って細胞内部のイオンが流出することにより,赤血球の破壊や細胞毒性など示します。
2.タンパク質毒素の構造と機能の解明
上に記したCEL-IIIのように,レクチンの中には細胞毒性を示すことで,外敵から身を守ることに役立っているものが多くあります。特に海産動物は陸上の動物と異なる興味ある構造や機能を持つ毒素タンパク質が存在していることから,本研究室ではそのような毒素タンパク質についても構造や機能を研究しています。現在までに,ラッパウニの叉棘(さきょく)などから数種類の毒素タンパク質遺伝子のクローニングを行い,その構造を明らかにしています。
3.超好熱菌由来酵素の構造・機能解明
超好熱菌は火山や海底熱水鉱床などの高温環境で生育し、それらが生産するタンパク質は高い耐熱性を有していることが知られている。また、超好熱菌のほとんどが生物の第3のドメインであるアーキアに属しており、新規代謝系・酵素が多く見出されている。そこで、それらの酵素の探索・有効利用の研究を進めている。その中で、超好熱菌由来酵素を遺伝子組換えタンパク質として大腸菌を宿主に用いて生産させると、酵素活性を示さないか、著しく低い活性しか示さないものが知られている。加熱によって酵素活性が活性化されるため、その時の構造変化の解明の研究を行っている。構造変化の解明にはX線結晶構造解析及びX線小角散乱測定を行っている。


サンプリング風景 X線小角散乱測定
4.膜タンパク質の立体構造解析
膜タンパク質のなかでも膜貫通タンパク質は生体膜内に存在し、物質輸送、情報伝達などの重要な機能をもっており、現在市販されている医薬品の七割程度が、その標的としていることが知られている。そのため、膜貫通タンパク質の立体構造の解明を行っている。
トランスポーターとは、生体膜を貫通し膜を通して物質の輸送をするタンパク質の事です。 近年、結晶化技術等の改良により各種膜蛋白質の結晶構造解析の報告が増加しつつある一方、依然として構造未知の原核生物由来トランスポーターは数多く、それらのトランスポートメカニズムの詳細は不明です。これらのトランスポーターの結晶構造解析による トランスポート機構の解明を目指し、研究に取り組んでいます。 その取り組みにおいて、蛋白質の発現量および精製時の安定性が結晶構造解析研究を行う際のボトルネックとなる場合が多く、それらの克服が結晶構造解析を成功に導くための重要な点であると言えます。現在、そのボトルネックである発現量および安定性の問題を克服するための、高発現トランスポーターの探索および精製の最適条件の検討を行っています。
これまでに本研究室で結晶構造解析されたタンパク質一覧
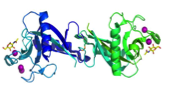
2-1 グミ( echinata)由来レクチン CEL-Iの構造解析 (2004年)pubmed:15319425 PDB ID: 1WMY 1WMZ
2-2 グミ(Cucumaria echinata)由来レクチン CEL-IIIの構造解析 (2004年)
pubmed: 15194688 PDB ID: 1VCL
2-3 グミ(Cucumaria echinata)由来レクチンCEL-IIIの糖複合体構造解析 (2007年)
pubmed: 17977832 PDB ID: 2Z48 2Z49
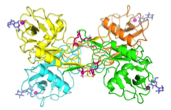
2-4 グミ(Cucumaria echinata)由来レクチン CEL-IV およびその糖複合体構造解析 (2011年)
pubmed:21247895 PDB ID: 3ALS 3ALT 3ALU
2-5 高熱菌(Sulfolobus shibatae)由来IPP イソメラーゼおよび基質複合体構造解析 (2009年)
pubmed:19158086 PDB ID: 2ZRU 2ZRV 2ZRW 2ZRX 2ZRY 2ZRZ
2-6 高熱菌(Sulfolobus shibatae)由来IPP イソメラーゼ-共有結合型阻害剤複合体構造解析(2011年)
pubmed: 22158896 PDB ID: 3B03 3B04 3B05 3B06
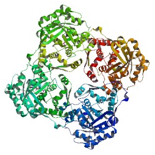
2-7 高熱菌(Sulfolobus shibatae)由来IPP イソメラーゼ8量体構造解析(2012年)
pubmed:22505674 PDB ID: 3VKJ
2-9 マウス由来カルノシナーゼCN2の構造解析(2008年)
pubmed:18550540 PDB ID: 2ZOF 2ZOG
2-10 西洋キク科由来アシルトランスフェラーゼDmATの構造解析構造解析 (2007年)
pubmed:17383962 PDB ID: 2E1T 2E1U 2E1V
2-11 マウス由来プロトンチャネルHv1 C末ドメインの構造解析 (2010年)
pubmed:20147290 PDB ID: 3A2A
2-12 日本脳炎ウイルスNS3 へリカーゼの構造解析 (2008年)
pubmed: 18201743 PDB ID: 2Z83
2-13 E型肝炎ウイルスORF2の構造解析 (2009年)
pubmed: 19620712 PDB ID: 2ZTN
|
Cucumaria echinata由来CEL-IIIの糖複合体構造 |
Cucumaria echinata由来CEL-I |
Cucumaria echinata由来CEL-IV |
高熱菌由来IPPイソメラーゼ |
||
|
E型肝炎ウイルスORF2 |
日本脳炎ウイルスへリカーゼ |
キク科アシルトランスフェラーゼ |
高熱菌由来IPPイソメラーゼ8量体構造 |
||
|
マウスカルノシナーゼCN2 |
マウスHv1 C末ドメイン |
To be continued …. |
|
||